Дистанційний центр хімічної освіти
|
Меню сайту
Наше опитування
Статистика
Онлайн всього: 1 Гостей: 1 Користувачів: 0 ...

Зворотній зв'язок
|
Лужні та лужноземельні елементиМаючи в зовнішньому електронному шарі тільки по одному електрону, що перебуває на порівняно великій відстані від ядра, атоми лужних елементів досить легко віддають електрон, тобто характеризуються низькою енергією йонізації. Зі сполук лужних металів широко розповсюджені в природі лише сполуки Натрію й Калію. У вигляді простих речовин у природі вони не зу стрічаються, тому що занадто активні. Найважливішими природними сполуками Натрію й Калію є: натрій хлорид (NaCl), натрій сульфат —мірабіліт (Na2SO4*10H2O), сильвініт (NaCl*KCl), карналіт (KCl*MgCl2*6H2O). Сполуки інших лужних металів зустрічаються дуже рідко. Францій отриманий штучно в ядерних реакціях. Лужні метали надзвичайно активні і є найсильнішими серед відомих відновників, тому електроліз водних розчинів солей цих металів не призводить до добування самих металів, а лише до утворення лугів. Прості речовини добувають електролізом розплавів їхніх галогенідів, найчастіше — хлоридів, що утворюють природні мінерали. Металічний натрій у промисловості добувають електролізом розплаву натрій хлориду з інертними (графітними) електродами. Фізичні властивості натрію й калію Натрій і калій — сріблясто-білі метали, що мають добру електропровідність; м’які, легші від води (плавають на її поверхні, реагуючи з нею). Хімічні властивості натрію й калію Натрій і калій активно взаємодіють із галогенами: 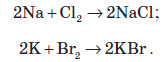 На повітрі натрій і калій активно згорають. Причому продуктом реакції є не оксиди, а пероксиди або надпероксиди: 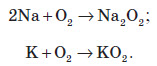 Як і всі лужні метали, натрій і калій активно взаємодіють із водою з утворенням водню та відповідних лугів. Калій найчастіше при такій взаємодії вибухає: 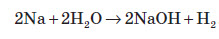 Застосування сполук натрію й калію Натрій та його сплав з калієм застосовують як рідкометалеві теплоносії. У металургії натрійметричним методом добувають низку туго плавких металів, а відновлюючи натрієм KOH, виділяють калій. Окрім того, натрій використовують як зміцнювальну добавку свинцевих сплавів. В органічному синтезі натрій використовують для добування багатьох речовин. Він слугує також каталізатором при добуванні деяких органічних полімерів. Із ртуттю натрій утворює твердий сплав — амальгаму натрію, яку іноді використовують як більш м’який відновник замість чистого металу. Натрій гідроксид застосовують для очищення продуктів переробки нафти, у миловарній, паперовій, текстильній та інших галузях промисловості, а також при виробництві штучного волокна. Калій потрібен у значній кількості для живлення рослин, тому його широко використовують як добриво у вигляді нітрату. Поташ K2CO3 використовують при виробництві скла та рідкого мила. Кальцій характеристика хімічного елемента Кальцій перебуває в головній підгрупі II групи, належить до лужноземельних металів разом з Барієм та Стронцієм. У зовнішній оболонці він має два електрони й може легко віддавати їх, утворюючи йони зі стійкими конфігураціями інертних газів. Поширеність у природі Кальцій має велику хімічну активність, тому зустрічається в природі тільки у вигляді сполук. Найважливіші природні сполуки Кальцію: а) вапняк, мармур, крейда (CaCO3); б) гіпс (CaSO4*2H2O); в) фосфорит і апатит (Ca3(PO4)2); г) доломіт (CaCO3*MgCO3). Фізичні властивості Кальцій — метал сріблясто-білого кольору, дуже легкий, як і лужні метали, але значно твердіший за них і має більш високу температуру плавлення (+851 °С). Кальцій зберігають під шаром гасу. Добування Кальцій добувають шляхом електролізу його розплавленого хлориду.
Хімічні властивості
Найважливішою сполукою Кальцію є його карбонат СаCO3. Він являє собою основну складову частину вапняку, мармуру, крейди, а також входить до складу доломіту (MgCO3*СаCO3). Кальцій карбонат використовують у виробництві цементу, сталі, скла. Кальцій та кальцій карбід застосовують в органічній хімії. А ще Кальцій відіграє дуже важливу роль у біохімічних процесах, які протікають у живих організмах. Магній застосовується для одержання легких сплавів, як відновник рідкісних металів і деяких неметалів (Si). Твердість води Твердість води — це природна властивість води, обумовлена присутністю в ній розчинених солей Кальцію та Магнію. Сумарну концентрацію йонів Магнію й Кальцію називають загальною твердістю води. Розрізняють постійну й тимчасову твердість води, їхня порівняльна характеристика подана в таблиці.
У склянки з водою
помістимо шматочки літію, натрію і калію. Калій від дотику з водою спалахує.
Натрій і літій реагують з водою менш повільно ніж калій. Поява малинового
забарвлення фенолфталеїну свідчить про утворення розчинів лугів. |
Форма входу
Пошук
Календар
Калькулятор
Анкета
|
||||||||||||||||||||||||||||||||||||||||||||