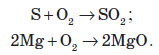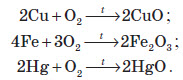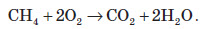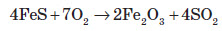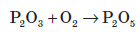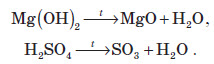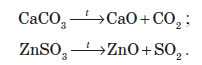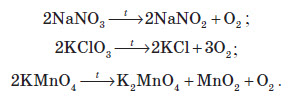Дистанційний центр хімічної освіти
|
Меню сайту
Наше опитування
Статистика
Онлайн всього: 1 Гостей: 1 Користувачів: 0 ...

Зворотній зв'язок
|
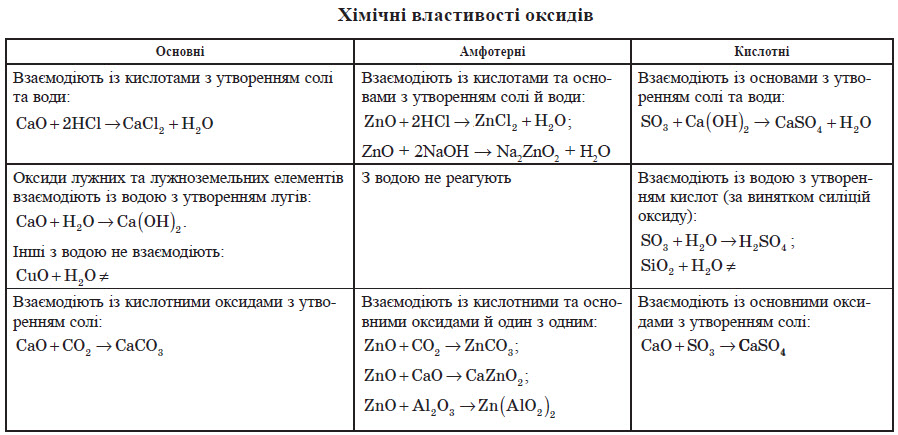
ОксидиОксиди — це складні речовини, що складаються з атомів двох хімічних елементів, один з яких Оксиген.Символ елемента Оксигену завжди записують на другому місці. Назви оксидів складаються з двох слів: перше — назва хімічного елемента, який утворює оксид, у називному відмінку, а друге — слово «оксид». Якщо елемент виявляє постійну валентність, то в назві оксиду його валентність не вказують: Na2O — натрій оксид; MgО — магній оксид; Al2O3 — алюміній оксид. Якщо елемент може виявляти різні валентності й утворювати кілька оксидів, то в назві оксиду після назви елемента вказують значення його валентності римською цифрою в дужках: CO — карбон (II) оксид; CO2 — карбон (IV) оксид; SO2 — сульфур (IV) оксид; SO3 — сульфур (VI) оксид. Назви оксидів неметалічних елементів іноді записують без зазначення валентності, а тільки вказуючи число атомів Оксигену в молекулі грецькими числівниками (моно, ді, три тощо). Наприклад, NO — нітроген монооксид, CO2 — карбон діоксид, SO3 — сульфур триоксид. Іноді співвідношення атомів не є цілими числами, у цьому разі ще використовують префікс «гемі», що означає «половина». Так, N2O — нітроген геміоксид (у цьому разі мається на увазі, що на один атом Нітрогену припадає половина атома Оксигену), N2O5 — нітроген геміпентаоксид (на один атом Нітрогену припадає «половина від п’яти», тобто два з половиною атоми Оксигену). Серед оксидів трапляються речовини і молекулярної, і немолекулярної будови. Структура оксидів обумовлює і їхні фізичні властивості. У більшості випадків оксиди неметалічних елементів мають молекулярну будову, а оксиди металічних елементів — немолекулярну будову. Оксиди металічних елементів мають немолекулярну будову. Це тверді речовини з високою температурою плавлення й кипіння. У більшості випадків вони не розчиняються у воді. Крім оксидів активних металічних елементів (лужних та лужноземельних металів), які активно реагують з водою. Оксиди, яким відповідають кислоти, називають кислотними оксидами. Більшість кислотних оксидів — це оксиди неметалічних елементів. Але кислотні оксиди здатні утворювати й металічні елементи, якщо ці елементи можуть виявляти дуже високі валентності, вищі, аніж 4. Так, до кислотних оксидів належать CrО3, Mn2O7, SO2, CO2, P2O5. Оксиди, яким відповідають основи, називають основними оксидами. До основних оксидів належать оксиди металічних елементів. Це, як правило, оксиди одно-, дво- і тривалентних металів. Na2O, CaO, MgO… Амфотерні оксиди – це оксиди які виявляють властивості кислотних та основних оксидів: ZnO, Al2O3, Cr2O3, Fe2O3… Кислотні ,основні та амфотерні оксиди утворюють групу солетворних оксидів. Відомі оксиди, яким не відповідає ані кислота, ані основа, їх називають несолетворними. До них належать карбон (ІІ) оксид CO, нітроген (ІІ) оксид NO, нітроген (I) оксид N2O та деякі інші. Вони являють собою гази, малорозчинні у воді, і не вступають із нею в хімічні реакції. Усі інші оксиди (кислотні й основні) називають солетворними. Добування оксидів Найбільш простий спосіб добування оксидів — це взаємодія простих речовин з киснем:
Майже всі прості речовини взаємодіють із киснем. Багато з них взаємодіють досить бурхливо, з виділенням великої кількості теплоти й світла, тобто горять.
Деякі прості речовини взагалі не реагують із киснем. Серед металів — це платина й золото, а серед неметалів — інертні гази (неон, аргон тощо) і галогени (хлор, бром, йод). Велика кількість складних речовин також здатні горіти в кисні. Під час горіння складної речовини утворюються оксиди всіх елементів, з яких складається ця речовина. Наприклад, унаслідок горіння метану CH4 утворюються два оксиди: карбон (IV) оксид та гідроген оксид:
Для промисловості велике значення мають реакції згорання сульфідів металів, тому що під час цих реакцій утворюються два цінних оксиди — сульфур (IV) оксид та оксиди металічних елементів. Останні використовують для добування чистих металів:
З киснем також можуть взаємодіяти деякі оксиди.
Оксиди можна добувати також розкладанням (дегідратацією) гідратів оксидів: гідратів кислотних оксидів (кислот) та гідратів основних оксидів (гідроксидів):
Оксиди також утворюються при розкладанні деяких солей оксигеновмісних кислот. При прожарюванні багатьох таких солей утворюються два оксиди: основний і кислотний (ангідрид кислоти, залишок якої утворює сіль).
Розкладанню при прожарюванні не піддаються солі Натрію та Калію. При нагріванні вони починають плавитися, а якщо й розкладаються, то за іншим принципом. Деякі із цих реакцій використовують у лабораторії для добування кисню:
Візьмемо оксиди
кремнію і фосфору. Це кислотні оксиди. Якщо кислотний оксид реагує з водою,
утворюється кислота, але не будь-який кислотний оксид може реагувати з водою.
Оксид фосфору і вода взаємодіють, утворюючи фосфорну кислоту. Лакмус червоніє у
кислому середовищі. Оксид кремнію, навіть при нагріванні не взаємодіє з водою. Лакмус не змінює кольору, кислота не утворюється. |
Форма входу
Пошук
Календар
Калькулятор
Анкета
|
||||||||||||||||||||||||||||||||||||||||||||