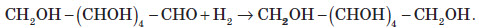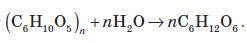Дистанційний центр хімічної освіти
|
Меню сайту
Наше опитування
Статистика
Онлайн всього: 1 Гостей: 1 Користувачів: 0 ...

Зворотній зв'язок
|
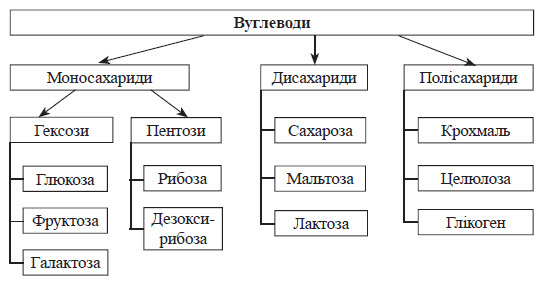
ВуглеводиЗагальна формула вуглеводів: Cn(H2O)m, однак це не означає, що вуглеводи складаються з вугілля та окремих молекул води. Ця формула відображає лише співвідношення атомів Карбону, Гідрогену та Оксигену в молекулах вуглеводів. І, власне, саме такому співвідношенню цей клас речовин зобов’язаний своєю назвою — (вугле)(води).
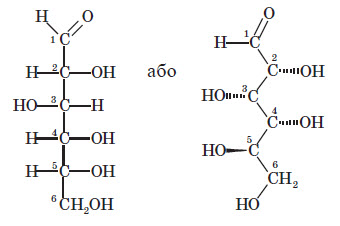
Глюкоза Глюкоза належить до альдегідоспиртів, тобто до складу її молекули входять два типи функціональних груп: альдегідна та спиртова (гідроксильна група).
Хімічні властивості глюкози 1. Комплексоутворення з купрум (ІІ) гідроксидом. Оскільки глюкоза є багатоатомним спиртом, вона проявляє якісну реакцію на багатоатомні спирти: взаємодія зі свіжоосадженим купрум (ІІ) гідроксидом. Як і у випадку із гліцеролом, при цьому утворюється складна комплексна сполука. 2. Утворення естерів. Як і всі спирти, глюкоза може вступати в реакцію естерифікації з кислотами. Причому як з органічними, так і з неорганічними. На практиці часто використовують п’яти оцтовий естер із глюкозою, реакцію утворення якого можна записати так: 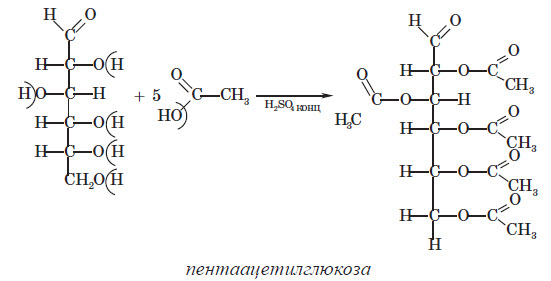 3. Відновлення глюкози з утворенням шестиатомного спирту — сорбіту:
4. Окиснення глюкози купрум (ІІ) гідроксидом або аміачним розчином аргентум гідроксиду: 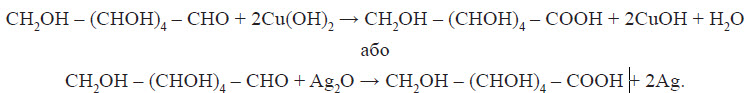 При цьому глюкоза (альдегідоспирт) окиснюється до глюконової кислоти (спиртокислота). 5. Бродіння глюкози. Спиртове бродіння використовують для добування спиртів. 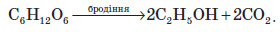 Під дією ферменту молочнокислих бактерій відбувається молочнокисле бродіння глюкози, при якому утворюється молочна кислота. 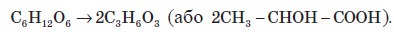 Глюкозу використовують як зміцнювальний лікувальний засіб, тому що її дуже легко засвоює організм й тому що вона дає йому енергію. Її також використовують для виготовлення лікувальних препаратів, при консервуванні крові, широко використовується в кондитерському виробництву, у виробництві дзеркал та іграшок, нею користуються при обробці й фарбуванні тканин і шкір. Сахароза Сахароза є представником дисахаридів, тому що її молекула складається із залишків двох вуглеводів — глюкози та фруктози: 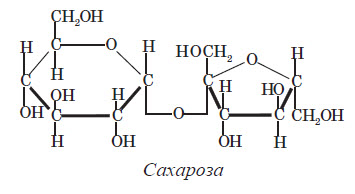 Сахароза являє собою білу кристалічну речовину, без запаху, добре розчинна у воді, солодка на смак, температура плавлення +180 °С. Хімічні властивості сахарози 1. Комплексоутворення: 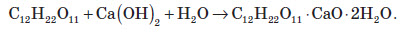 2. Гідроліз: 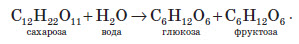 Добування сахарози із цукрового буряка Насамперед, потрібно найбільш повно добути цукор з буряка за допомогою води. Задля цього буряк у механічних бурякорізках перетворюють на тонку стружку й обробляють її водою в дифузорах, добуваючи цукор. З отриманого розчину ще не можна безпосередньо виділити цукор, тому що домішки, які надходять із буряка,— органічні кислоти, білки, барвники тощо,— сильно забруднюють цукор і заважають його кристалізації. Отже, далі постає найбільш складне завдання — очистити розчин сахарози від домішок. Для цього його насамперед обробляють вапняним молоком. Під дією кальцій гідроксиду органічні кислоти та інші домішки осаджуються з розчину. Тим часом сахароза залишається в розчині, тому що дає з кальцій гідроксидом розчинний сахарат. Із сахарату знову потрібно виділити сахарозу. Цього досягають шляхом обробки розчину карбон (IV) оксидом, який осаджує кальцій карбонат. Звільнений від осаду розчин цукру випарюють і піддають кристалізації. Так виходить цукровий пісок. Частина його після додаткового очищення йде на виробництво рафінаду. Крохмаль і целюлоза Фізичні властивості крохмалю і целюлози Крохмаль — це аморфний порошок з характерним хрускотом (картопляного крохмалю), нерозчинний у воді у звичайних умовах. При потраплянні в гарячу воду зерна крохмалю сильно набухають, їхні оболонки розриваються, утворюється колоїдний розчин. Целюлоза являє собою волокнисту речовину білого кольору, нерозчинну у воді. На відміну від крохмалю, целюлоза зовсім не взаємодіє з водою навіть при кип’ятінні. Чиста целюлоза в нашому житті зустрічається у вигляді вати. Будова молекул крохмалю й целюлози Найпростіша формула крохмалю (і целюлози) — (C6H10O5) . У цій формулі значення n — від кількох сотень до кількох тисяч. Отже, крохмаль — це природний полімер, що складається з багаторазово повторюваних структурних ланок C6H10O5. Він складається з молекул двох типів. Із цієї причини крохмаль навіть вважають сумішшю двох речовин — амілози та амілопектину. Амілоза (її в крохмалі 20% має лінійні молекули й більш розчинна. Молекули амілопектину (його 80% розгалужені, і він менш розчинний у воді. Ці молекули відрізняються й за відносною молекулярною масою: для лінійних молекул (амілози) вона сягає близько сотень тисяч, для розгалужених молекул (амілопектину) — кількох мільйонів. Найпростіша й молекулярна формули целюлози аналогічні до формул крохмалю. Очевидно, що при однаковому складі ці речовини істотно відрізняються за властивостями. Порівняно із крохмалем у целюлози більш висока відносна молекулярна маса. Молекули крохмалю складаються із залишків а -глюкози, а целюлози — із залишків молекул b-глюкози. У цьому також полягає причина відмінностей хімічних властивостей крохмалю та целюлози. Хімічні властивості крохмалю й целюлози 1. Комплексоутворення крохмалю з йодом. Властивість крохмалю утворювати синє забарвлення з йодом використовують як якісну реакцію для виявлення крохмалю. З йодом реагує здебільшого амілоза, утворюючи забарвлену сполуку. Молекула амілози у вигляді спіралі оточує молекули йоду, при цьому навколо кожної молекули йоду виявляється шість глюкозних залишків. Нагрівання руйнує такий комплекс, і забарвлення зникає. 2. Гідроліз.
3. Термічне розкладання. При нагріванні деревини до високої температури без доступу повітря виділяється досить велика кількість продуктів. Окрім вуглецю й води, утворюються рідкі продукти, зокрема й метиловий спирт (який саме тому й називають деревним спиртом), ацетон, оцтова кислота. 4. Естерифікація. Найбільше значення мають естери целюлози з нітратною кислотою (нітроцелюлоза) та оцтовою кислотою (ацетилцелюлоза).
Застосування крохмалю Крохмаль — це основний вуглевод нашої їжі. Для добування глюкози крохмаль нагрівають із розведеною сульфатною кислотою впродовж кількох годин. Якщо процес гідролізу не доводити до кінця, то в результаті утворюється густа солодка маса — суміш декстринів та глюкози — патока. Декстрини, добуті з крохмалю, використовують як клей. Крохмаль застосовують для накрохмалювання білизни: під дією нагрівання гарячою праскою він перетворюється в декстрини, які склеюють волокна тканини й утворюють щільну плівку, що охороняє тканину від швидкого забруднення. Крім того, це полегшує наступне прання, оскільки часточки бруду, зв’язані з декстринами, значно легше змиваються водою. Крохмаль використовують для виробництва етилового спирту. Під час цього процесу його спочатку гідролізують під дією ферменту, який міститься в солоді, а потім продукт гідролізу збро джують у присутності дріжджів у спирт. Етиловий спирт, який використовують для промислових потреб (синтез каучуку), добувають синтетичним шляхом з етилену та гідролізом целюлози. Застосування целюлози Завдяки своїй механічній міцності целюлоза в складі деревини використовується в будівництві, з неї виготовляють усілякі столярні вироби. У вигляді волокнистих матеріалів (бавовни, льону, коноплі) її використовують для виготовлення ниток, тканин, канатів. Виділена з деревини (звільнена від супутніх речовин), целюлоза йде на виготовлення паперу. Естери целюлози використовують для виготовлення нітролаків, кіноплівки, медичного колодію, штучного волокна та вибухових речовин. Крохмаль одержують найчастіше з картоплі. Для цього картоплю подрібнюють, промивають водою і перекачуют в великі ємкості, де відбувається відстоювання. Одержаний крохмаль ще раз промивають водою, відстоюють і висушують в струмені теплого повітря.
У пробірці
знаходиться аміачний розчин нітрату срібла, а в колбі розчин глюкози.
Приливаємо глюкозу до арґентум нітрату, нагріваємо пробірку. Виділяється
металічне срібло на стінках пробірки і утворюється дзеркало. |
Форма входу
Пошук
Календар
Калькулятор
Анкета
|
||||||||||||||||||||||||||||||||||||||||||||