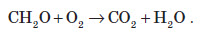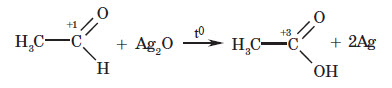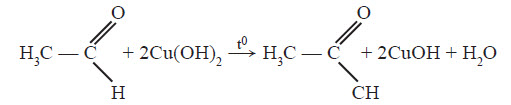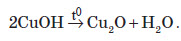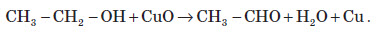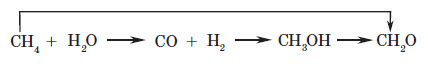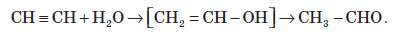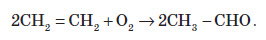До альдегідів належать сполуки, які у своєму складі містять альдегідну групу. Альдегідна група є функціональною групою альдегідів: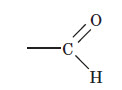
Скорочено альдегідну групу записують: −CHO. Найпростішим альдегідом є мурашиний альдегід, у молекулі якого до альдегідної групи приєднаний атом Гідрогену, його молекулярна формула — CHO2.
Зв’язки атома Карбону в альдегідній групі аналогічні до зв’язків у ненасичених вуглеводнях: три його валентні електронні хмари в стані sp2-гібридизації утворюють зв’язки із двома атомами Гідрогену (в інших альдегідах — з атомами Гідрогену й Карбону) і з атомом Оксигену.
З’єднані подвійним зв’язком атоми Оксигену й Карбону мають різну електронегативність. Унаслідок цього область перекривання електронів (область найбільшої електронної густини) зміщена до атома Оксигену. Таким чином, подвійний зв’язок C = O поляризований: 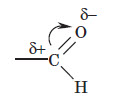
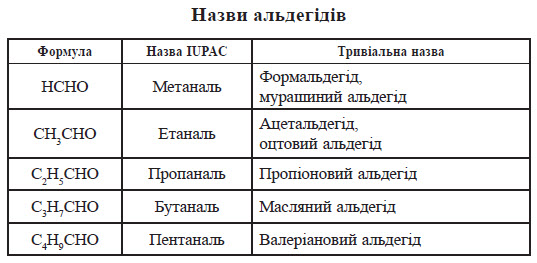
Загальна формула насичених альдегідів CnH2nO.
Альдегіди — безбарвні речовини, з характерним запахом. Перший член гомологічного ряду альдегідів — формальдегід — при звичайних умовах є газоподібною речовиною (на відміну від спиртів). Хімічні властивості альдегідів
1. Горіння.
���
3. Окиснення альдегідів (реакція «срібного дзеркала»).
Аналогічно до аргентум оксиду купрум (ІІ) гідроксид здатний окиснювати альдегіди. При цьому утворюється жовтий осад одновалентного купрум (І) гідроксиду:
При подальшому нагріванні відбувається розклад купрум (І) гідроксиду й утворення червоного осаду одновалентного купрум (І) оксиду:
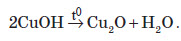
Добування альдегідів
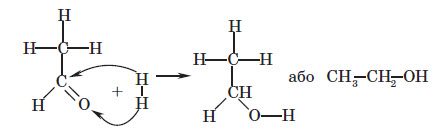
1. Окиснення спиртів.
2. Окиснення метану.
Метод добування формальдегіду з метану складається, в основному, з кількох стадій:
1) шляхом взаємодії метану з водною парою добувають водний газ (суміш водню й карбон (ІІ) оксиду CO); 2) із нього синтезують метиловий спирт;
3) потім спирт окиснюють у мурашиний альдегід:
3. Реакція Кучерова.
4. Окиснення етилену киснем.
Застосування альдегідів
Формальдегід
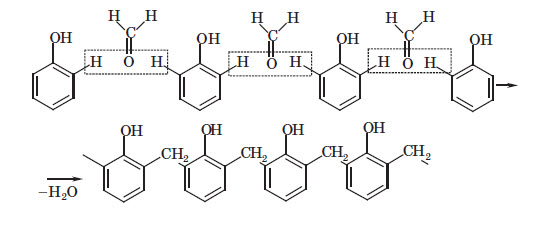
Застосовують у виробництві термореактивних пластмас, феноло-формальдегідних та сечовино-формальдегідних смол. Формальдегід є біологічно активною речовиною: під його впливом відбувається згортання (денатурація) білка. На цьому ґрунтується його (точніше його водного розчину — формаліну) застосування як засобу для дезінфекції, як дубильного засобу та консерванта для анатомічних препаратів. Формаліном називають 37—40% водний розчин формальдегіду, до якого як інгібітор полімеризації додають 6—15% метанолу. У медицині також використовують похідні формальдегіду — гексаметилентетрамін (уротропін).
Ацетальдегід
Найважливіші застосування оцтового альдегіду ґрунтуються на використанні його реакцій окиснення та відновлення. За допомогою першої з них добувають оцтову кислоту, за допомогою другої у деяких країнах — етиловий спирт. Основне застосування оцтового альдегіду — добування оцтової кислоти.