Металічні елементи займають в основному ліву нижню частину Періодичної системи хімічних елементів Д. І. Менделєєва. До металічних елементів належать ті елементи, в чиїх атомах на зовнішньому електронному рівні перебуває невелике (від одного до чотирьох) число електронів, які атоми можуть легко віддавати.
Такі спільні фізичні властивості металів обумовлені наявністю в металів особливого типу хімічного зв’язку — металічного. Наявність таких властивостей, як електропровідність і теплопровідність, указує на значну рухливість електронів у металах.
Атоми металів на зовнішньому електронному рівні мають невелику кількість електронів, які досить слабко взаємодіють з ядром, отже, можуть легко віддаватися. Таким чином, кожний атом металу віддає в спільне користування щонайменше по одному електрону зі свого зовнішнього електронного рівня. Усі електрони можуть вільно переміщатися по всьому металічному кристалу й утворюють так званий «електронний газ».
Присутністю вільних електронів та їхнім рухом по всьому зразку металу пояснюється значна електропровідність, теплопровідність металів та їхній характерний металічний блиск.
Чим більша активність металу, тим енергійніше він реагує з іншими речовинами. За активністю всі метали можна розташувати в ряд, який називають рядом активності металів, або витискувальним рядом металів, або рядом напруг металів, а також електрохімічним рядом напруг металів. Цей ряд уперше дослідив видатний український учений М. М. Бекетов, тому цей ряд називають також рядом Бекетова.
Ряд активності металів Бекетова має такий вигляд (наведені найбільш уживані метали):
K > Ca > Na > Mg > Al > Zn > Fe > Ni > Sn > Pb > H2 > Cu > Hg > Ag > Au.
У цьому ряді метали розташовані за зменшенням їхньої активності. Серед наведених металів найбільш активний калій, а найменш активний — золото. За допомогою цього ряду можна визначити, який метал активніший від іншого. Також у цьому ряді присутній водень. Звісно ж, водень не є металом, але в цьому ряді його активність прийнята за точку відліку (своєрідний нуль).
Загальні хімічні властивості металів
В атомах металів на зовнішній електронній оболонці утримується невелике число електронів. Ці електрони порівняно легко можуть відриватися від атомів. Така особливість металів є причиною не тільки їхніх фізичних, але й хімічних властивостей. Виходячи з того, що метали здатні тільки віддавати електрони зовнішнього електронного рівня, можна зробити висновок, що в хімічних реакціях метали здатні проявляти тільки властивості відновника.
Основний процес, який характеризує хімічні властивості металів, можна записати у вигляді такої схеми:
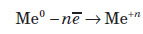
Взаємодія металів з неметалами
Більшість металів активно реагують із неметалами, при цьому метали виконують роль відновника, а неметали — окисника. У результаті реакцій утворюються бінарні сполуки: солі безоксигенових кислот:
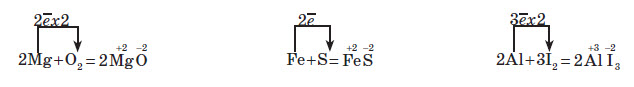
Або в загальному вигляді:
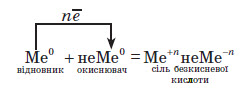

Взаємодія металів з кислотами
Активні метали, які розташовані в ряді напруг до водню, витискують Гідроген із розчинів кислот.
Метали, які розташовані в ряді напруг після водню, з розчинами кислот (окрім нітратної та сульфатної) не взаємодіють:
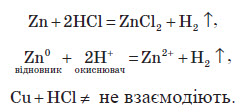
Якщо метал здатний проявляти кілька ступенів окиснення, то при взаємодії з безоксигеновою кислотою утворюється сіль, у якій метал, як правило, має нижчий ступінь окиснення, наприклад:
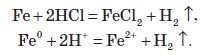
Взаємодія металів із солями
Більш активні метали здатні витісняти менш активні з їхніх солей:
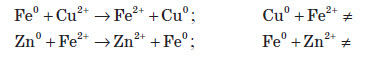
Загальні способи добування металів
лабораторні методи добування
а) відновлення оксидів металів воднем; таким способом зазвичай добувають не дуже активні метали, які не взаємодіють із воднем:
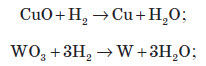
б) розкладання оксидів важких металів:
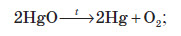
в) витіснення металів з їхніх солей більш активними металами:
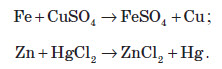
Добування металів у промисловості
а) відновлення оксидів металів вуглецем або кремнієм:
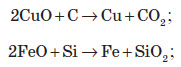
б) відновлення оксидів металів карбон монооксидом:
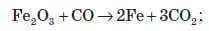
в) відновлення металів з оксидів більш активними металами в розплавах:
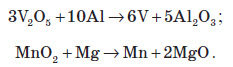
Відновлення металів з оксидів більш активними металами називають металотермічним методом. Найпоширенішим металом, що його використовують як відновник, є алюміній (алюмінотермія).
Корозія металів
Корозією зазвичай називають мимовільне руйнування металів у результаті їхньої хімічної й електрохімічної взаємодії із зовнішнім середовищем та перетворення їх у стійкі сполуки (оксиди, гідроксиди, солі).
Власне кажучи, корозія являє собою сукупність окисно-відновних процесів, які відбуваються при контакті металів з агресивним середовищем, що призводить до руйнування металевих виробів. Під агресивним середовищем мають на увазі окисну атмосферу (присутність кисню в атмосфері Землі робить її окисною), особливо в присутності води або розчинів електролітів.
За механізмом процесу розрізняють хімічну та електрохімічну корозію металів. Хімічна корозія являє собою звичайну хімічну реакцію між атомами металів і різних окисників. Прикладами хімічної корозії є високотемпературне окиснення металів киснем, окиснення поверхні алюмінію на повітрі, взаємодія металів із хлором, сіркою, сірководнем H2S тощо.
Електрохімічна корозія протікає в розчинах, тобто, в основному, при контакті металів з розчинами електролітів, особливо у тих випадках, коли метали перебувають у контакті з менш активними металами. Швидкість корозії істотно залежить від активності металів, а також від концентрації й природи домішок у воді. У чистій воді метали майже не піддаються корозії, а в контакті з більш активними металами навіть у розчинах електролітів не кородують.
Сумарне рівняння реакції корозії заліза можна записати так:
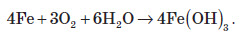
На сьогодні існує кілька способів запобігання корозії.
Відокремлення металу від агресивного середовища — фарбування, змащування маслами, покриття неактивними металами або емаллю (І). Приведення поверхні металів у контакт із більш активними металами (ІІ). Використання речовин, що сповільнюють корозію (інгібітори корозії), та сплавів, стійких до корозії (ІІІ).
I. Найпростіший спосіб захистити сталь від корозії — це ізолювати метал від атмосферного повітря. Це можна зробити за допомогою масляного, жирового змащування або нанесення захисного шару фарби.
Зараз широко застосовують захисні покриття з органічних полімерів. Покриття можна робити різних кольорів, і це досить гнучке розв’язання проблеми корозії. Навіть побіжний погляд на речі, які оточують нас у побуті, дає масу прикладів такого розв’язання: холодильник, сушарка для посуду, піднос, велосипед тощо.
II. Іноді залізо покривають тонким шаром іншого металу. Деякі виробники виготовляють кузови автомобілів зі сталі з гальванічним цинковим покриттям. При такій обробці утворюється міцно зчеплений з основою шар цинк оксиду, і якщо гальванічне покриття не ушкоджене, воно добре захищає від іржі.
Дуже розповсюдженим розв’язанням проблеми захисту від корозії є використання іржостійких сплавів. Багато зі сталевих виробів, використовуваних у побуті, особливо ті, що перебувають у постійному контакті з водою: кухонний посуд, ложки, виделки, ножі, бак пральної машини тощо — виготовлені з іржостійкої сталі, яка не вимагає додаткового захисту.
Сплави
Сплав — це суміш металу з одним або кількома компонентами. Компоненти змішують при плавці; при застиганні матеріалу утворюється однорідний твердий матеріал. Через присутність інших хімічних елементів у складі сплавів властивості металів змінюються, і часто новий матеріал стає більш міцним.
Так, додавання до сталі марганцю підвищує її зносостійкість, що дозволяє використовувати її для виготовлення залізничних рейок. А додавання хрому збільшує стійкість до корозії; таку сталь називають іржостійкою.
У доменній печі протікає величезна кількість реакцій, які поділяють на кілька груп.
1-ша група реакцій.
Горіння коксу й утворення відновника — карбон (II) оксиду. Сьогодні в домни, окрім повітря, надходить природний газ, який інтенсифікує процес плавки й дозволяє зменшувати ви трату дорогого коксу:
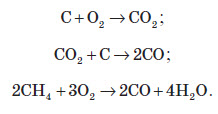
Відновлення ферум (III) оксиду карбон (II) оксидом протікає трьома послідовними стадіями:
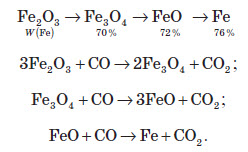
3-тя група реакцій.
Відновлення домішок. Завдяки цій групі реакцій багато елементів порожньої породи переходять у чавун:
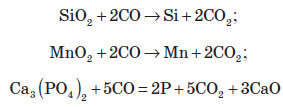
Утворення чавуну найчастіше описують за допомогою рівняння реакції між залізом та коксом, а також між залізом та чадним газом:
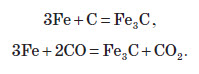
5-та група реакцій.
Утворювані в процесі плавки силікати, алюмосилікати, алюмінати, деякі сульфіди утворюють побічний продукт доменного виробництва — шлак. Він відзначається невеликою густиною й тому накопичується на поверхні чавуну, запобігаючи його окисненню.
Хімічні реакції, які перебувають в основі переробки чавуну в сталь
1-ша група реакцій. При виплавці чавуну протікають реакції відновлення Феруму, а при переробці чавуну в сталь — реакції окиснення домішок. Подібно до того як у доменному процесі протікали небажані процеси відновлення домішок, так і при виплавці сталі відбувається небажана реакція — окиснення Феруму. Слід зазначити, що атмосфера в сталеплавильних печах є окисною. У ній міститься повітря, кисень та пари води. Саме вони й спричинюють окиснення Феруму, перетворення його в ферум (II) оксид, що можна зобразити рівнянням:
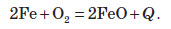
Доведено, що при виплавці сталі ніякий інший ферум оксид не утворюється. Більше того, якщо в сталеплавильну піч помістити оксиди Fе3O4 або Fе2О3, що містяться в залізній руді або в іржі металобрухту, то вони реагують із залізом як окисники, утворюючи все той же ферум (II) оксид:
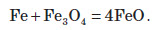
2-га група реакцій. Окиснення домішок (кремнію, марганцю, фосфору) ферум (II) оксидом протікає за типом заміщення. Утворювані оксиди, крім CO, являють собою пористі тверді речовини й тому поступово спливають на поверхню сталі. Окиснення вуглецю спричинює в розплаві ефект кипіння, що викликане виділенням пухирців газу карбон (II) оксиду. Їхній рух відіграє позитивну роль, оскільки сприяє перемішуванню металу, очищенню від шлаку, що утворився в ньому, а також від пухирців азоту й водню.
3-тя група реакцій. До неї входять процеси усунення сполук Сульфуру й Фосфору негашеним вапном СаО. Для більш повного зв’язування зазначених домішок вапно використовують не тільки для футерування внутрішніх поверхонь печей, але й як добавки до сталі. Кальцій оксид при цьому вступає в такі реакції: